Olomoucký objev odhaluje příčinu rezistence nádorů vůči nové generaci léčiv
Repro: Žurnál UP
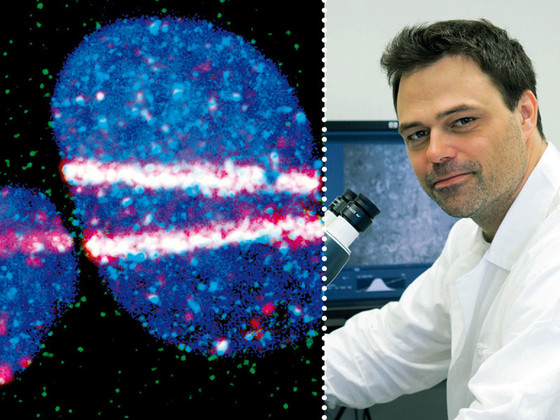
Nový mechanismus, kterým rakovinné buňky odolávají protinádorové léčbě, identifikovali vědci z Ústavu molekulární a translační medicíny (UMTM) lékařské fakulty ve spolupráci s nizozemskými kolegy. Nadějné výsledky výzkumu, který může přispět k cílenější terapii rakoviny vaječníků a karcinomu prsu, potvrdil tým nejcitovanějšího českého vědce Jiřího Bártka v olomouckých laboratořích. Studii zveřejnil prestižní vědecký časopis Nature.
Práce se zaměřuje na nádory, jejichž vznik způsobuje genetická dispozice k dědičnému onemocnění rakovinou vaječníků nebo prsu. Zodpovídá za ni gen BRCA1, který je u postižených jedinců od narození mutován v jedné ze svých dvou kopií. „Podstatným způsobem se tím zvyšuje riziko, že dojde i k mutaci druhé kopie. Zdravá buňka tím přijde o schopnost bezchybně opravovat DNA poškození a k opravám začne využívat záložního mechanismu, který velkou měrou akumuluje mutace. Buňka se pak začne měnit v nádorovou,“ popsal člen mezinárodního týmu a spoluautor studie Martin Mistrík z olomouckého pracoviště.
Pro léčbu karcinomu vaječníků s genetickými mutacemi BRCA1 byl do klinické praxe nedávno uveden nový lék olaparib, který buňkám zablokuje záložní opravný systém. „Zdravé buňky to téměř nepocítí, zatímco buňky nádorové začnou hromadit DNA poškození s fatálními důsledky,“ uvedl Mistrík. Slibný směr protinádorové terapie ale časem zkomplikovalo zjištění, že mezi miliony různě zmutovaných nádorových buněk se najdou takové, které léčbě vzdorují, dokáží se adaptovat a stanou se příčinou relapsu. Po přechodném zlepšení se tak nemoc vrací v podobě, která je vůči léku odolná.
Jeden ze způsobů, kterým těmto buňkám umožňuje „vypnout“ a přežít léčbu olaparibem, objevil tým profesora Rottenberga z Netherland Cancer Institute. Experimentem na geneticky upravených myších s BRCA1 mutací prokázal, že jedním z faktorů, kterým se buňky stanou vůči léku rezistentní, je ztráta regulačního proteinu REV7, známého také jako MAD2L2.
Ověření na lidských buňkách se ujal právě profesor Jiří Bártek a jeho olomoucká laboratoř. Její experimentální práce zároveň pomohly odhalit hledaný molekulární mechanismus, kterým nádorové buňky léčbě odolávají. „Série experimentů v pracovištích ÚMTM zahrnula nejrůznější genové manipulace spojené s pokročilou mikroskopií. Ukázala, že REV7 má zcela nečekanou novou funkci jakéhosi přepínače mezi opravnými systémy poškozené DNA,“ uvedl Mistrík.
Vědci předpokládají, že pro pacienty a pro řešení závažného problému rezistence na protinádorovou léčbu bude mít olomoucký objev významné důsledky. „Očekáváme, že REV7 jako biomarker umožní přesněji předpovědět terapeutickou odpověď na celou skupinu PARP inhibitorů a poslouží k lepšímu výběru nejvhodnějších pacientů,“ zdůraznil Mistrík. Výsledky výzkumu zároveň představují výrazný příslib pro další vývoj látek k cílenější protinádorové léčbě a s minimálními nežádoucími účinky na zdravé tkáně.

„Studium mechanismů nádorové rezistence je velmi důležité pro nalezení alternativních způsobů léčby. Této problematice se na ÚMTM dlouhodobě věnujeme a publikace výsledků v takto prestižním časopise je nejlepším důkazem jejich významu a kvality," zhodnotil studii ředitel ÚMTM Marián Hajdúch.
Pro vkládání komentářů je nutné se přihlásit/zaregistrovat.
Komentáře nevyjadřují stanovisko redakce ani vydavatele. Redakce diskusi nemoderuje, ale vyhrazuje si právo nevhodné komentáře smazat, případně zrušit registraci.